Хімічні властивості лугів та нерозчинних гідроксидів
Повторимо вивчене раніше
Для цього виконайте завдання на сайті "Всеосвіта"
Хімічні властивості оксидів
Щоб доєднатися перейдіть за посиланням https://vseosvita.ua/go
введіть код: ffn784
або перейдіть за посиланням:
https://vseosvita.ua/test/start/ffn784
або Відскануйте QR-код
за допомогою смартфона:Та ще одненьке завдання
Хімічні властивості кислот
Щоб доєднатися перейдіть за посиланням https://vseosvita.ua/go
введіть код: dnt205
або перейдіть за посиланням:
або Відскануйте QR-код
за допомогою смартфона:
ОПОРНИЙ КОНСПЕКТ ЗТЕМИ: Запишіть у зошит
З параграфа 33 виписати визначення понять Індикатори,реакція нейтралізації, реакція обміну
Також виписати Таблицю 10, схеми реакцій в рамочках, с. 175 табличку "Умови перебігу реакцій обміну у водних розчинах"
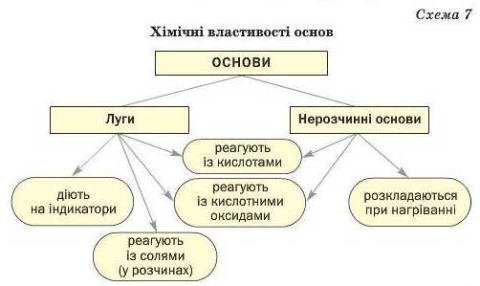


Після вивчення сьогоднішньої теми ви повинні знати
хімічні властивості основ, визначення реакції нейтралізації; вміти складати
рівняння реакцій за участю основ, аналізувати й порівнювати властивості.
Виконайте Лабораторний дослід №2 та №3 Можна по підручнику с. 177-178 (оцінка буде менша), а можна за моєю інструктивною карткою (на оцінку 12)
Інструктивна картка
«Хімічні
властивості основ»
Уважно
прочитайте завдання, зрозумійте його, а потім виконайте, дотримуючись правил
ТБ!
Дослід 1 Дія лугів (розчинних основ) на індикатори
Візьміть три пробірки. У кожну з них налийте
по 1 мл розчину натрій гідроксиду NaOH.
Додайте кілька крапель розчину: у 1 –лакмусу; у 2 – метилоранжу; у 3 –
фенолфталеїну.
Що спостерігаєте? Який
висновок можна зробити?
Зробіть запис в опорну схему «Хімічні властивості основ» (п.1): вкажіть
назву досліду, назви речовин, що реагують та утворюються.
Дослід 2 Взаємодія лугів (розчинних основ) з кислотами
У пробірку налийте 1
мл розчину натрій гідроксиду NaOH. Додайте 1-2 краплі фенолфталеїну, а потім – розчин сульфатної кислоти H2SO4 (обережно!)
Що спостерігаєте? Про
що свідчить зміна забарвлення?
Зробіть запис в опорну схему (п. 2) ): вкажіть назву досліду, клас
речовин, що реагують та утворюються.
Закінчіть рівняння реакцій (для
допомоги використайте § п. «Реакції з кислотами»)
З’ясуйте, як
називаються реакції між основами і кислотами.
Дослід 3 Взаємодія лугів (розчинних основ) з кислотними оксидами.
У пробірку налийте 1
мл розчину кальцій гідроксиду Са(ОН)2. Через скляну трубку декілька
секунд видихайте (обережно!)
вуглекислий газ СО2 у розчин.
Що спостерігаєте? Про
що свідчить поява осаду?
Зробіть запис в опорну схему (п.3) ): вкажіть назву досліду, клас
речовин, що реагують та утворюються.
Закінчіть рівняння реакцій (для допомоги
використайте § п. « Реакції з кислотними оксидами»)
Дослід 4 Розкладання нерозчинних основ при нагріванні
У порцелянову чашку насипте купрум (ІІ)
гідроксид Cu(OH)2, що знаходиться у
пробірці. Чашку поставте на кільце штативу та нагрівайте (обережно!) за допомогою спиртівки. Зверніть увагу на зміну
забарвлення речовини. Про що це свідчить?
Зробіть
запис в опорну схему (п. 4)
): вкажіть назву досліду, клас речовин, що реагують та утворюються.
Закінчіть рівняння реакцій (для допомоги використайте § п.
«Термічний розклад»)
Дослід 5 Взаємодія нерозчинних основ з кислотами.
До
купрум (ІІ) гідроксиду Cu(OH)2 , що знаходиться у пробірці долийте (обережно!) трохи розчину (1-2 мл)
хлоридної кислоти HCl .
Що відбувається з
осадом? Про що це свідчить?
Зробіть запис в опорну схему (п. 5) ): вкажіть назву досліду, клас
речовин, що реагують та утворюються.
Закінчіть рівняння реакцій,
використовуючи для допомоги § п. «Реакції з кислотами».
З’ясуйте, як називаються реакції між основами і
кислотами.
Опорна схема
«Хімічні властивості основ»
лугів
(розчинних основ)
|
нерозчинних
основ
|
|||||||||||||||||||||||||||||||||||||||
1.__________________________________

Лакмус
Метилоранж |
4.___________________________________
Cu(OH)2 =
Al(OH)3 =
|
|||||||||||||||||||||||||||||||||||||||
2.__________________________________
NaOH + H2SO4 =
Ca(OH)2 + HCl =
|
5.___________________________________
Cu(OH)2 + HCl =
Al(OH)3 + H2SO4 =
|
|||||||||||||||||||||||||||||||||||||||
3.___________________________________
Ca(OH)2 + CO2 =
KOH + SO3 =
|
||||||||||||||||||||||||||||||||||||||||
Виконайте тести результати занесіть в таблицю
І
варіант
1.Назвіть сполуку Ca(OH)2
2.MgO, Mg(OH)2, CO2,
NaOH, HNO3, Cr(OH)3
а)оксиди;
б)кислоти;
в)основи
3.a/KOH
б/Cu(OH)2
в/Fe(OH)3
4.Zn(OH)2
5.a/NaOH, Na2CO3,
Al2O3
б/KOH, ZnCl2, HNO3
в/LiOH, Mg(OH)2, Cu(OH)2
6.a/Fe(OH)3
б/NaOH
в/Ca(OH)2
7.a/Zn(OH)2
б/Cu(OH)2
в/Ba(OH)2
8.а/жовтий
б/малиновий
в/синій
9.а/кислот з металами
б/кислот з основами
в/оксидів між собою
10.а/Cu(OH)2
б/NaOH
в/Ca(OH)2
11.а/калій оксид
б/сульфатна кислота
в/карбон(ІV) оксид
12.а/калій гідроксид
б/карбон(ІV) оксид
в/кальцій оксид
ІІ
варіант
1. Назвіть сполуку
Fe(OH)2
2.
MgS, H2SO4, Ba(OH)2,
KOH, K2CO3, Al(OH)3
а/оксиди
б/кислоти
в/солі
3. a/Fe(OH)3
б/CsOH
в/Ca(OH)2
4. Cr(OH)3
5. a/H2SO4, KOH, NaCl
б/Ca(OH)2, Pb(OH)2, NaOH
в/Al(OH)3, AlCl3, Al2O3
6. a/Mg(OH)2
б/Ca(OH)2
в/LiOH
7. a/NaOH
б/Cr(OH)2
в/Al(OH)3
8. а/малиновий
б/жовтий
в/синій
9 .а/основ з
кислотами
б/оксидів з кислотами
в/розклад нерозчинної основи
10.а/Fe(OH)2
б/LiOH
в/Ba(OH)2
11.а/хлоридна
кислота
б/сульфур (VІ) оксид
в/магній оксид
12.а/барій
гідроксид
б/хлорид на кислота
в/калій оксид
ІІІ
варіант
1. Назвіть сполуку Cr(OH)3
2. Na2O,
NaOH, Al2O3, ZnO, HCl, Mg(OH)2
a/оксиди
б/кислоти
в/основи
3. a/NaOH
б/Cr(OH)3
в/Cr(OH)2
4. Fe(OH)2
5. a/NaOH, Na2CO3,
Al2O3
б/KOH, ZnCl2, HNO3
в/LiOH, Mg(OH)2, Cu(OH)2
6. a/Ba(OH)2
б/NaOH
в/Cr(OH)2
7. a/Zn(OH)2
б/Cu(OH)2
в/Ba(OH)2
8.
а/малиновий
б/синій
в/жовтий
9.а/кислот з металами
б/кислот з основами
в/оксидів між собою
10. a/KOH
б/Ba(OH)2
в/Cr(OH)3
11. а/калій оксид
б/сульфатна кислота
в/карбон (ІV) оксид
12. а/калій гідроксид
б/карбон (ІV) оксид
в/кальцій оксид
ІV варіант
1. Назвіть сполуку Al(OH)3
2. H2SO4,
KOH, HCl, Cr(OH)3, HNO3, CO2
а/оксиди
б/кислоти
в/основи
3. a/KOH
б/Ca(OH)2
в/LiOH
4. NaOH
5. a/H2SO4, KOH, NaCl
б/Ca(OH)2, Pb(OH)2, NaOH
в/Al(OH)3, AlCl3, Al2O3
6. a/Cu(OH)2
б/Ca(OH)2
в/KOH
7. a/NaOH
б/Cr(OH)2
в/Al(OH)3
8. а/синій
б/жовтий
в/малиновий
9. а/основ з кислотами
б/оксидів з кислотами
в/розклад нерозчинних основ
10. а/NaOH
б/LiOH
в/Al(OH)3
11. а/хлорид на кислота
б/сульфур (VІ) оксид
в/магній оксид
12. а/барій гідроксид
б/хлорид на кислота
Кількість
балів
|
І
варіант
|
ІІ
варіант
|
ІІІ
варіант
|
|
0,5
|
1 кальцій гідроксид
|
1 ферум(ІІ)гідроксид
|
1 хром(ІІІ)гідроксид
|
1 алюміній гідроксид
|
0,5
|
2 в
|
2 в
|
2 а
|
2 б
|
0,5
|
3 в
|
3 а
|
3 б
|
3 б
|
0,5
|
4 ІІ
|
4 ІІІ
|
4 ІІ
|
4 І
|
0,5
|
5 в
|
5 б
|
5 в
|
5 б
|
0,5
|
6 а
|
6 а
|
6 в
|
6 а
|
1
|
7 в
|
7 а
|
7 в
|
7 а
|
1
|
8 б
|
8 а
|
8 а
|
8 в
|
1
|
9 б
|
9 а
|
9 б
|
9 а
|
2
|
10 а
|
10 а
|
10 в
|
|
2
|
11 б
|
11 а
|
11 б
|
11 а
|
2
|
12 а
|
12 б
|
12 б
|
12 б
|
Домашнє завдання
Повторити параграф 31, с. 158 №7-9 задачі
Повторити параграф 32, с. 171 №1-5 письмово, вивчити параграф 33, с. 180 №6-8 письмово
Зворотній зв’язок
Всі завдання виконувати в робочому зошиті, обов’язково писати дату виконання завдання. Фото виконаних завдань присилати мені особистими повідомленями у VIBER (0955320031) або на електронну пошту vvn1602@gmail.com
Строк виконання завдання 20.03.2020 року. Кожного наступного дня оцінка буде нижчою.
Обов’язково!
Залиште коментар під дописом завдання
Обов’язково!
Залиште коментар під дописом завдання
Немає коментарів:
Дописати коментар